Publicat pe 5 august 2021
Actualizat pe 9 martie 2022
Amiodarona, un medicament antiaritmic de clasa III, are efecte multiple asupra depolarizării și repolarizării miocardice, care îl fac un medicament antiaritmic extrem de eficient. Cu toate acestea, amiodarona este asociată cu o serie de efecte secundare, inclusiv disfuncție tiroidiană (atât hipo-, cât și hipertiroidism), care se datorează conținutului ridicat de iod al amiodaronei și efectului său toxic direct asupra tiroidei.

Conținut
Cum acționează amiodarona?
Amiodarona conține doi atomi de iod. Se estimează că metabolismul amiodaronei în ficat eliberează aproximativ 3 mg de iod anorganic în circulația sistemică la 100 mg de amiodaronă ingerată. Conținutul mediu de iod într-o dietă tipică americană este de aproximativ 0,3 mg / zi. Astfel, 6 mg de iod asociat cu o doză de 200 mg de amiodaronă crește semnificativ încărcarea zilnică de iod.
Amiodarona este foarte lipofilă și este concentrată în țesutul adipos, mușchiul cardiac, scheletal și tiroida. Eliminarea din corp are loc cu un timp de înjumătățire de aproximativ 100 de zile. Prin urmare, toxicitatea amiodaronei poate apărea și după retragerea medicamentului.
Efectele amiodaronei asupra funcției tiroidiene pot fi împărțite în acele efecte care au proprietăți intrinseci ale medicamentului și acele efecte care se datorează iodului.
Efectele intrinseci ale amiodaronei
- Amiodarona inhibă inelul exterior 5′-monodeiodarea tiroxinei (T4), scăzând astfel producția de triiodotironină (T3); revers T3 se acumulează deoarece nu este metabolizat în T2.
- Amiodarona (și în special metabolitul desetilamiodaronă) blochează legarea receptorilor T3 de receptorii nucleari și scade expresia unor gene legate de hormonii tiroidieni.
- Amiodarona poate avea un efect toxic direct asupra celulelor foliculare tiroidiene, ceea ce duce la o tiroidită distructivă.
Efectele datorate iodului
Iodul reprezintă un substrat pentru sinteza hormonilor tiroidieni. Se transportă activ în celulele foliculare tiroidiene și se organizează pe reziduuri de tirozil din tiroglobulină.
Autoreglarea normală a iodului împiedică indivizii normali să devină hipertiroidieni după expunerea la o încărcătură de iod (de exemplu, radiocontrast). Când concentrațiile de iod intratiroidian ating un nivel ridicat critic, transportul de iod și sinteza hormonilor tiroidieni sunt inhibate tranzitoriu până când depozitele de iod intratiroidian revin la niveluri normale (efectul Wolff-Chaikoff).
Cu toate acestea, pacienții cu boală tiroidiană de bază prezintă defecte în autoreglarea iodului:
- Pacienții cu boală tiroidiană autoimună „nu reușesc să scape” de efectul Wolff-Chaikoff. Rezultatul este dezvoltarea gușei și hipotiroidismului în boala Hashimoto și ameliorarea hipertiroidismului în boala Basedow-Graves.
- Pacienții cu zone de autonomie într-o gușă nodulară nu autoreglează iodul și adăugarea mai multor doze poate duce la sinteza excesivă a hormonilor tiroidieni și tirotoxicoză (Jod-Basedow).
Riscul disfuncției tiroidiene
Atât hipo-, cât și hipertiroidismul sunt complicații ale terapiei cu amiodaronă. Într-o meta-analiză a patru studii randomizate care au implicat 1465 de pacienți eutiroidieni, prevalența bolii tiroidiene clinice a fost mai mare la pacienții care au primit terapie cu amiodaronă în comparație cu placebo.
În alte recenzii și rapoarte, riscul de disfuncție tiroidiană indusă de amiodaronă variază de la 2 la 30 %, în funcție de starea tiroidiană subiacentă a unui individ, de aportul de iod din dietă și de cazurile de tulburări subclinice ale tiroidei.
Funcția tiroidiană subiacentă – Efectele clinice ale amiodaronei asupra funcției tiroidiene la orice individ depind de starea de bază a glandei tiroide a acelui individ.
Normală
La persoanele normale, eutiroidiene care primesc amiodaronă, modificările acute ale testelor funcției tiroidiene includ:
- Concentrațiile serice de T4 și fT4 cresc cu 20 până la 40% în prima lună de tratament.
- Concentrațiile serice de T3 scad cu până la 30% în primele câteva săptămâni de tratament.
- Concentrațiile serice de rT3 cresc cu 20% la scurt timp după inițierea terapiei.
- Concentrația serică de TSH crește de obicei ușor după inițierea tratamentului și poate depăși limita superioară a normalului.
După trei până la șase luni de tratament, se ajunge la o stare de echilibru la majoritatea pacienților care au fost eutiroidieni la momentul inițial: - Concentrația serică de TSH se normalizează
- Concentrațiile serice de T4 total, T4 liber și rT3 rămân ușor ridicate sau în intervalul normal superior
- Concentrațiile serice de T3 rămân în intervalul normal scăzut
Amiodarona poate provoca, de asemenea, o tiroidită distructivă la pacienții fără boală tiroidiană subiacentă.
Anormală
- Pacienții cu boală tiroidiană autoimună subiacentă sunt mai predispuși să dezvolte hipotiroidism indus de amiodaronă, probabil din cauza eșecului de a scăpa de efectul Wolff-Chaikoff.
- La pacienții cu gușă multinodulară subiacentă sau cu boala latentă Basedow-Graves, poate apărea hipertiroidism (sinteză crescută a T4 și T3). Excesul de iod din amiodaronă oferă un substrat crescut, rezultând o producție sporită de hormoni tiroidieni.
Aportul alimentar de iod – Aportul alimentar de iod afectează, de asemenea, riscul unei disfuncții tiroidiene induse de amiodaronă:
- În zonele cu iod suficient, hipotiroidismul indus de amiodaronă pare a fi mai frecvent decât hipertiroidismul.
- În schimb, hipertiroidismul indus de amiodaronă este mai frecvent decât hipotiroidismul în regiunile cu deficit de iod.
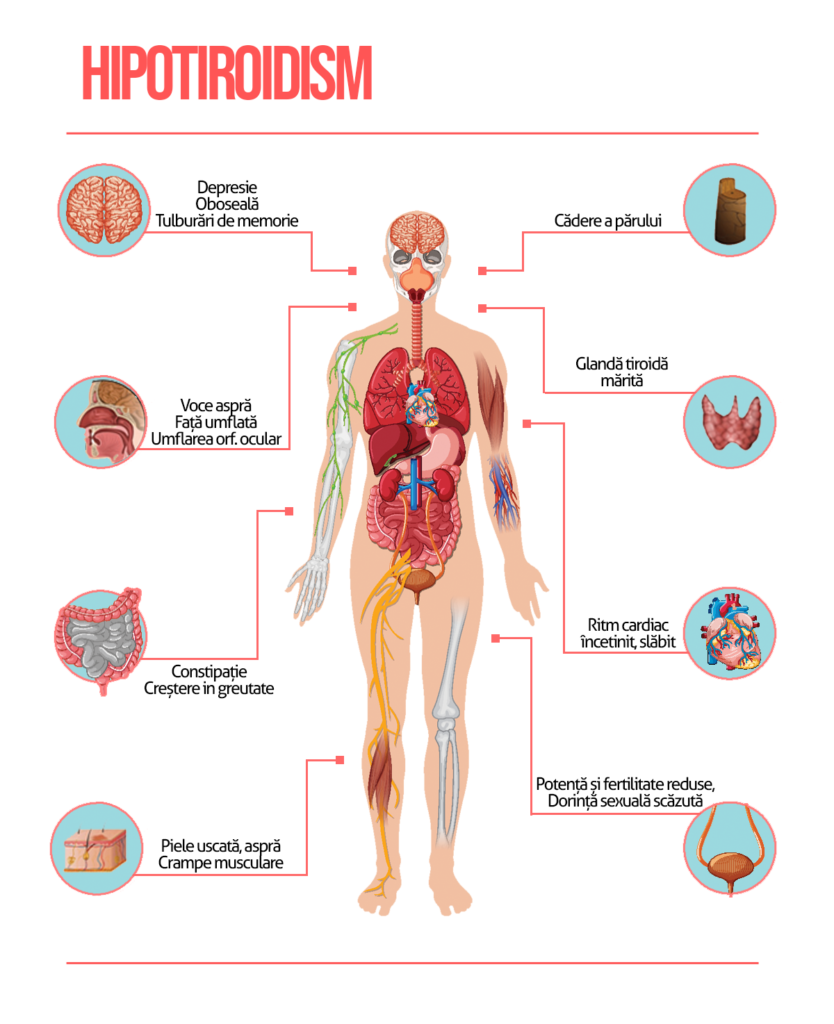
Hipotiroidism
Epidemiologie
Modificările tranzitorii ale testelor funcției tiroidiene apar adesea la persoanele eutiroidiene tratate cu amiodaronă. Cu toate acestea, majoritatea pacienților rămân eutiroidieni în timpul tratamentului cu amiodaronă (89% într-un studiu). Într-un studiu, hipotiroidismul manifest (TSH> 10 mU / L) s-a dezvoltat la 5% dintre pacienții cărora li s-a administrat amiodaronă, dar hipotiroidismul subclinic (TSH 4,5-10 mU / L) s-a dezvoltat cu încă 25% în plus.
Pacienții cu tiroidită Hashimoto subiacentă sau anticorpi antitiroidieni pozitivi sunt mai predispuși să dezvolte hipotiroidism persistent. Această observație poate explica prevalența mai mare a hipotiroidismului indus de amiodaronă la femei comparativ cu bărbații.
În zonele cu iod suficient, hipotiroidismul indus de amiodaronă este mai frecvent decât hipertiroidismul și poate apărea la până la 20% dintre pacienții tratați cu amiodaronă. În schimb, hipertiroidismul indus de amiodaronă este mai frecvent decât hipotiroidismul în regiunile cu deficit de iod.
Sarcina
Hipotiroidismul tranzitor poate să apară la sugarii femeilor tratați cu amiodaronă în timpul sarcinii. De exemplu, într-un studiu realizat pe 64 de sarcini în care amiodarona a fost administrată mamei, 11 sugari (17%) au prezentat hipotiroidism tranzitoriu; 2 din cei 11 aveau gușă . Hipotiroidismul a fost tranzitoriu în toate cazurile și doar cinci sugari au fost tratați pe termen scurt cu hormoni tiroidieni.
Manifestări clinice
Manifestările clinice și diagnosticul hipotiroidismului asociat amiodaronei sunt similare cu cele ale hipotiroidismului din orice cauză. Hipotiroidismul și simptomele hipotiroidiene se pot dezvolta după două săptămâni sau la 39 de luni de la inițierea terapiei cu amiodaronă.
Diagnostic
Pacienții trebuie să aibă funcția tiroidiană evaluată la câteva săptămâni după începerea amiodaronei și la fiecare câteva luni după aceea pentru dezvoltarea hipotiroidismului manifest, în special la cei cu dovezi de autoimunitate înainte de inițierea amiodaronei. Hipotiroidismul trebuie diagnosticat pe baza valorii TSH seric înainte ca pacientul să prezinte simptome.
Deoarece la pacienții cu eutiroidie se observă creșteri mici ale concentrațiilor serice de TSH (10-20 mU / L) în primele trei până la șase luni de la inițierea tratamentului cu amiodaronă, hipotiroidismul indus de amiodaronă va fi diagnosticat numai atunci când concentrațiile serice de T4 sunt spre limita inferioară a normalului sau scăzute sau când creșterea ușoară a TSH persistă.
Tratament
Funcția tiroidiană poate fi ușor normalizată prin substituirea cu T4 (levotiroxină) în timp ce amiodarona este continuată.
Scopul terapiei este de a restabili concentrația serică de TSH la normal, ținând cont de faptul că poate fi necesară o doză mai mare decât cea obișnuită din cauza efectelor probabile ale amiodaronei asupra metabolismului T4 și producției T3 și, eventual, asupra acțiunii hormonului tiroidian. Pacientul trebuie retestat dacă amiodarona este sistată la o dată ulterioară.
Amiodarona nu este de obicei întreruptă, cu excepția cazului în care nu reușește să controleze aritmia subiacentă. Cu toate acestea, dacă amiodarona este oprită, hipotiroidismul la pacienții fără boală tiroidiană preexistentă aparentă se rezolvă adesea. În schimb, hipotiroidismul poate persista după sistarea amiodaronei la pacienții cu tiroidită cronică autoimună subiacentă cu titruri ridicate de anticorpi antitiroidieni peroxidazici (TPO) și gușă și, prin urmare, necesită terapie permanentă cu T4.
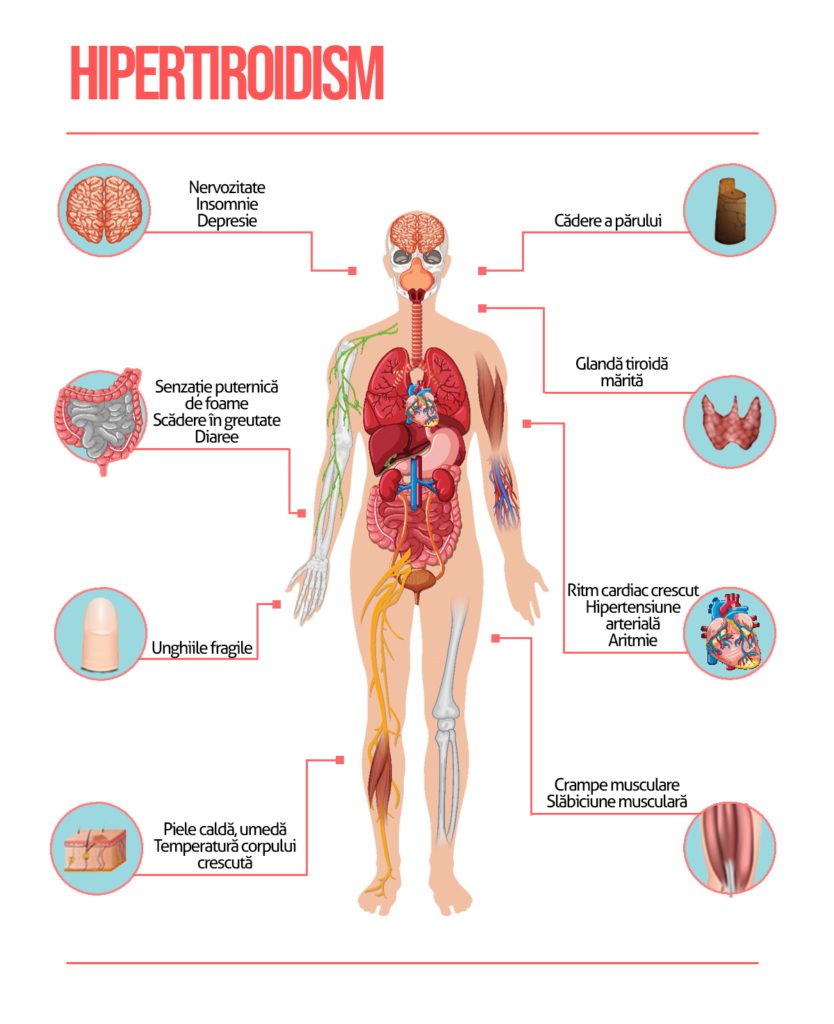
Hipertiroidism
Tipuri de hipertiroidism
Există două tipuri de tirotoxicoză indusă de amiodaronă (AIT). În tipul I, există o sinteză crescută a hormonului tiroidian, în timp ce în tipul II, există un exces de eliberare de T4 și T3 datorită tiroiditei distructive. Aceste tipuri diferă în ceea ce privește patogeneza, managementul și rezultatul.
- Tipul I – În AIT de tip I, există hipertiroidism cu sinteză crescută a T4 și T3. Acest tip este de obicei observat la pacienții cu gușă multinodulară preexistentă sau cu boala latentă Basedow-Graves; excesul de iod din amiodaronă asigură un substrat crescut, rezultând o producție sporită de hormoni tiroidieni. În timp ce majoritatea acestor pacienți au gușă multinodulară veche, unii pacienții care au boala Basedow-Graves latent, aceasta poate deveni evidentă după expunerea la cantități mari de iod.
- Tipul II – În AIT de tip II, hipertiroidismul este o tiroidită distructivă care are ca rezultat eliberarea în exces de T4 și T3, fără o sinteză hormonală crescută. Apare de obicei la pacienții fără boală tiroidiană subiacentă și este cauzată de un efect toxic direct al amiodaronei asupra celulelor epiteliale foliculare tiroidiene.
Faza hipertiroidiană poate dura de la câteva săptămâni la câteva luni și este adesea urmată de o fază hipotiroidiană cu eventuală recuperare la majoritatea pacienților, dar nu la toți. Din motive neclare, efectele toxice ale medicamentului pot dura doi până la trei ani pentru a deveni manifeste.
În multe cazuri, există forme mixte de AIT, ceea ce face atât diagnosticul, cât și tratamentul dificil Riscul oricărui tip crește odată cu dozele cumulative mai mari.
Prevalență
Prevalența AIT, precum și distribuția pe tip (I sau II), variază în funcție de regiunea geografică. Se crede că acest lucru se datorează în primul rând diferențelor în aportul alimentar de iod:
- În Statele Unite, 3 până la 5% dintre pacienții tratați cu amiodaronă devin hipertiroidieni, de obicei între patru luni și trei ani de la inițierea medicamentului. Majoritatea cazurilor sunt de tip II.
- În regiunile cu deficit de iod, AIT este mai frecvent decât în Statele Unite, apare la aproximativ 10-12% dintre pacienții cu AIT de tip I predominând de obicei.
Cu toate acestea, distribuția cazurilor în funcție de tip se poate schimba, după cum se arată într-un raport de 215 pacienți consecutivi cu AIT observați la o singură instituție din Italia de peste 26 de ani. În 1980, comparativ cu 2006, 2 din 6 (40 la sută) versus 12 din 14 (86 la sută) din noile cazuri de AIT au fost de tip II. Explicațiile posibile pentru această observație includ aportul îmbunătățit de iod din regiune și evitarea amiodaronei la pacienții cu boală tiroidiană cunoscută.
Manifestări clinice
Manifestările clinice ale hipertiroidismului indus de amiodaronă sunt adesea mascate deoarece activitatea sa betablocantă minimizează multe dintre manifestările adrenergice ale excesului de hormoni tiroidieni și posibil deoarece metaboliții amiodaronei pot bloca legarea T3 la receptorul său nuclear.
Simptomele și semnele prezente frecvente includ dezvoltarea sau reaparația aritmiilor atriale; exacerbarea bolii cardiace ischemice sau a insuficienței cardiace; sau pierdere inexplicabilă în greutate, neliniște sau febră.
Pacienții cu hipertiroidism indus de amiodaronă au o rată de trei ori mai mare a evenimentelor cardiovasculare adverse majore (în principal aritmii ventriculare) comparativ cu pacienții eutiroidieni. Prezența unei disfuncții ventriculare stângi severe la pacienții cu hipertiroidism indus de amiodaronă (tip I sau tip II) poate fi asociată cu creșterea mortalității.
Diferențierea celor două tipuri
Distincția dintre tipul I și tipul II este critică, deoarece terapia diferă pentru cele două tipuri. Cu toate acestea, distincția poate fi dificilă utilizând criterii clinice, parțial pentru că unii pacienți pot avea combinate ambele mecanisme. Testele funcției tiroidiene nu sunt utile pentru diferențierea tipului I de hipertiroidismul de tip II.
Tipul I, atunci când este văzut în cadrul unui nodul sau gușă autonomă subiacentă, tinde să apară devreme după începerea tratamentului cu amiodaronă (la o medie de 3,5 luni într-un studiu), în timp ce tipul II apare mult mai târziu (mediana de 30 de luni). Când tirotoxicoza apare inițial după ce amiodarona a fost întreruptă (19% din AIT în acest studiu), este mult mai probabil să fie de tip II (95% în acest studiu).
La pacienții care nu iau amiodaronă, absorbția radioiodului este principalul test utilizat pentru a face distincția între tiroidita subacută distructivă și hipertiroidismul asociat cu sinteza de novo a hormonului tiroidian; absorbția de 24 de ore a iodului radioactiv este <1 % în tiroidita subacută și crescută sau normală în gușa nodulară toxică sau boala Basedow-Graves.
Cu toate acestea, ingestia zilnică de 6 mg sau mai mult de iod biodisponibil din amiodaronă are ca rezultat niveluri serice suficient de ridicate de iod care concurează cu trasorul utilizat pentru efectuarea testului de absorbție. Prin urmare, majoritatea pacienților cu tipul I (precum și toți pacienții cu tipul II) au absorbții mai mici de 1%.
Criteriile utilizate pentru a încerca diferențierea tipul I de hipertiroidismul de tip II sunt:
- Dacă absorbția de iod radioactiv de 24 de ore este detectabilă, sugerează AIT de tip I.
- Pacienții cu tip I au deseori gușă multinodulară sau gușă difuză, în timp ce cei cu tip II nu au de obicei gușă sau un gușă difuză mică.
- În două studii, concentrațiile serice de tiroglobulină au fost mai mari, iar concentrațiile serice de interleukină-6 au fost mai mici la pacienții cu hipertiroidism de tip I. Într-un al treilea studiu, concentrațiile de interleukină-6 nu au fost utile pentru a distinge tipul I de tipul II.
- Două studii au raportat că sonografia Doppler color (CFDS) poate distinge hipertiroidismul de tip I (vascularizație crescută) de tipul II (vascularizație absentă); 80 la sută dintre pacienți ar putea fi clasificați prin CFDS. Cu toate acestea, interpretările CFDS în hipertiroidismul asociat amiodaronei necesită un sonograf cu experiență.
- Două rapoarte au utilizat captarea tiroidei tehnetiu-99m (99mTc) -sestamibi și scintigrafie pentru a distinge tipul I (normal sau crescut) de tipul II (scăzut) și au constatat că acest lucru este mai util decât CFDS.
- Prezența anticorpilor receptorilor de tirotropină sugerează boala Basedow-Graves.
Dr. Cristina Cînpeanu ⬤
Medic Specialist – Endocrinologie
- Specializare: Endocrinologie
- Peste 9 ani experiență
- A ajutat peste 55 de oameni pe Medic Chat
- Feedback excelent
- Răspunsuri rapide (tipic <2 ore)
- Peste 35 testimoniale
- Medic endocrinolog și specialist în nutriție endocrină, nutriție clinică și comunitară, certificată în: puncție-biopsie tiroidiană ecoghidată, evacuare chist tiroidian sub ghidaj ecografic, elastografie tiroidiană, ecografie endocrină, densitometrie osoasă, scintigrafie, RMN, CT endocrine, terapia infertilității, managementul obezității, tulburările de dinamică sexuală și ovarul polichistic
“Sunteţi un doctor uimitor, am primit răspunsul în 10 minute! Pot spune că iubiţi cu adevărat ceea ce faceţi și sunteţi o persoană plină de grijă și empatică. Vă voi recomanda cu drag!” (Rujan)
“Vă mulțumesc pentru grija și timpul acordat pentru a explica complexitatea situatiei în termeni clari” (Luciana)
